CIENCIAS NATURALES Y EXACTAS: INVESTIGACIÓN
Cápsulas de alginato para la protección de polifenoles presentes en el aceite esencial de orégano
Muchiutti, Gabriela Silvina*; López Novello, Luciano Hernan*; Córsico, Francisco Armando* y Larrosa, Virginia Judit**
* Universidad Nacional de Entre Ríos (Argentina).
** Universidad Nacional de Entre Ríos - Conicet (Argentina).
Contacto: larrosa_v@hotmail.com
DOI: https://doi.org/10.33255/3059/687
Este artículo proviene de los resultados del PID NOVEL 9072 Aprovechamiento de propiedades antioxidantes y antibacterianas del aceite esencial de orégano mediante desarrollo de técnicas innovadoras: Micro - encapsulación y Películas biodegradables. Facultad de Bromatología. UNER-11/2014 Aprobación del Informe Final por RESOLUCIÓN «C.S.» 270/16. (28-09-16)- 05/2016.
Recibido el 13/06/2018
y aceptado el 24/07/2019.
Resumen
Se evaluó el alginato de sodio como material encapsulante del aceite esencial de orégano, aplicando la técnica de gelificación iónica del alginato de sodio y calcio. Se estudió mediante un diseño bifactorial, en el cual se adoptaron dos niveles para la distancia de caída y para los tiempos de retención en los procesos de elaboración. El aceite esencial se obtuvo de orégano seco de la variedad Origanum majorana, empleando un aparato de tipo Clevenger. La liberación del aceite esencial en agua se cuantificó mediante polifenoles totales determinados espectrofotométricamente según el procedimiento de Folin-Ciocalteau. La evaluación de alginato de sodio como material encapsulante indicó que las cápsulas con mayor contenido de aceite esencial fueron las obtenidas por proceso de mayor distancia y menor tiempo de retención. Se concluyó qué alginato de sodio es adecuado para formar cápsulas de aceite esencial de orégano y podrían incluirse en productos alimenticios.
Palabras clave: Orégano; Aceite esencial; Cápsula; Alginato; Polifenoles; Liberación.
Abstract
Alginate capsules for protecting polyphenols present in oregano essential oil
Sodium alginate was evaluated as an encapsulating material of oregano essential oil, applying the ionic gelation technique of sodium and calcium alginate. It was studied through a bifactorial design, in which two levels were adopted for the distance of fall and for the retention times in the elaboration processes. The essential oil was obtained from dehydrated oregano of the Origanum majorana variety, using a Clevenger type apparatus. The release of the essential oil in water was quantified by spectrophotometrically determined total polyphenols according to the Folin-Ciocalteau procedure. The evaluating sodium alginate as encapsulant material indicated that capsules with higher content of essential oil were obtained by process a greater distance and shorter retention time. It was concluded which sodium alginate is suitable for constituting oregano essential oil capsules and could be included in food products.
Keywords: Oregano; Essential oil; Capsule; Alginate; Polyphenols; Release.
Resumo
Cápsulas de alginato para a proteção de polifenóis presentes no óleo essencial de orégano
O alginato de sódio foi avaliado como material encapsulante do óleo essencial de orégano, aplicando a técnica de gelificação iônica do alginato de sódio e cálcio. Foi estudado usando um desenho de dois fatores, no qual foram adotados dois níveis para a distância de queda e para os tempos de retenção nos processos de elaboração. O óleo essencial foi obtido de orégano seco da variedade Origanum majorana, utilizando um aparelho de tipo Clevenger. A liberação do óleo essencial em água foi quantificada por polifenóis totais determinados espectrofotometricamente de acordo com o procedimento de Folin- Ciocalteau. A avaliação do alginato de sódio como material encapsulante indicou que as cápsulas com maior teor de óleo essencial foram as obtidas pelo processo de maior distância e menor tempo de retenção. Concluiu-se que o alginato de sódio é adequado para a formação de cápsulas de óleo essencial de orégano e pode ser incluído em produtos alimentícios.
Palavras-chave: Orégano; Óleo essencial; Cápsula; Alginato; Polifenóis; Liberação.
I. Introducción
La encapsulación es una técnica en la que se retienen gotitas de un compuesto de interés en una matriz de encapsulación diseñada para proteger y permitir la liberación del compuesto en diferentes momentos, condiciones o zonas del tracto digestivo (Champagne y Fustier, 2007). Consiste en la preparación de una emulsión que depende de ciertos parámetros, tales como la fase volumétrica dispersa, el contenido de sólidos totales y la proporción de material de la pared, los cuales influyen sobre las características y propiedades funcionales de las cápsulas. Asumiendo como objetivo aislar el material del núcleo de los efectos deteriorantes del oxígeno, retardar la evaporación de un núcleo volátil, controlar la velocidad a la que deja la cápsula, mejorar las propiedades de manejo de un material pegajoso, enmascarar el sabor o el olor del núcleo, aislar un núcleo reactivo del ataque químico y, finalmente, diluir el material del núcleo cuando debería usarse en cantidades muy pequeñas (Shahidi y Han, 1993; Gharsallaoui et al., 2007). El alginato es un hidrocoloide adecuado para la encapsulación por ser biocompatible, no tóxico y degradable. Entre las sales de alginato más empleadas se han encontrado la de sodio, debido a su alta solubilidad en agua fría y característica transición sol-gel de forma instantánea e irreversible ante el ión calcio (Funami et al., 2009). Posee propiedades gelificantes, estabilizantes y espesantes, razones por las cuales ha sido de gran interés para la industria alimentaria. La encapsulación con alginato de sodio se conoce como gelificación iónica, donde el alginato se usa como un material encapsulante que, al contacto con una solución de catión divalente o polivalente, forma un hidrogel al instante. Esta facilidad de producción permite tener una técnica de encapsulado con buenas perspectivas de aplicación industrial, no solo por el bajo costo de los materiales formadores de hidrogel, sino, además, por las mínimas pérdidas durante la gelificación iónica una vez establecidas las mejores condiciones de proceso.
Los alimentos vegetales y sus aceites esenciales son uno de los principales grupos de alimentos que tienen efecto antioxidante; son compuestos volátiles naturales con un fuerte olor, formado por plantas aromáticas como metabolitos secundarios. Desde la Edad Media se han usado ampliamente para aplicaciones antimicrobianas, medicinales y cosméticas, en especial hoy en día son utilizados por las industrias farmacéutica, sanitaria, cosmética, agrícola y alimentaria (Guimarães et al., 2010; Bozin et al., 2006; Celiktas et al., 2007). Tradicionalmente el orégano se ha consumido como una especia; sin embargo, recientemente hay más interés en otros usos potenciales, particularmente como el aceite esencial, que ha demostrado ser un buen agente antioxidante.
Informes relacionados con O. vulgare (Pizzale et al., 2002) han asociado el contenido de compuestos fenólicos con la actividad antioxidante. Lagouri et al. (1993) publicaron una investigación sobre actividades antioxidantes de aceites esenciales de diversas plantas aromáticas, donde demostraron que el aceite esencial de orégano, rico en timol y carvacrol, tenía un considerable efecto antioxidante en el proceso de oxidación de la manteca. La encapsulación de aceites esenciales se constituye en una tecnología interesante utilizada en la industria de alimentos, al prevenir su volatilización y extender la vida útil de estos componentes biológicos (Gonzales-Molina et al., 2010). El objetivo de este estudio fue la evaluación del alginato de sodio como material encapsulante del aceite esencial de orégano con el fin de proteger los polifenoles presente.
II. Materiales y métodos
II.1. Aceite esencial de orégano
Extracción
La materia prima utilizada fue orégano seco de la variedad conocida como Origanum x majoricum, obtenida de la cosecha del cultivo en el distrito de Gualeguaychú, provincia de Entre Ríos en Argentina.
El aceite esencial de orégano (aeo) fue extraído de las partes aéreas (hojas) de las plantas seleccionadas por el método de hidrodesatilación, usando un aparato de tipo Clevenger (Dadalioğlu y Evrendilek, 2004). La mezcla de agua-aceite se recogió en un embudo de separación, se centrifugó, se secó sobre sulfato de sodio anhidro y se almacenó en recipientes de vidrio sellados cubiertos con papel de aluminio a 4 °C hasta su uso.
II.2. Encapsulación del aceite esencial de orégano
Formación de cápsulas
El agente de encapsulación utilizado fue una solución acuosa de alginato de sodio al 1 % (p/v) (BioChemica, Reino Unido). Las cápsulas se elaboraron utilizando la técnica de gelificación iónica de alginato de sodio y cloruro de calcio, por el método de goteo por gravedad (Deladino et al., 2008). Las cápsulas se obtuvieron mezclando, mediante un agitador magnético, el aceite esencial de orégano (componente activo, ca) con la solución acuosa de alginato de sodio (3 % v/v). Una vez homogeneizada, la solución de alginato se dejó caer desde una bureta a 50 ml de solución de cloruro de calcio (0,05 M). Las cápsulas formadas se mantuvieron en la solución de cloruro de calcio, con el propósito de fortalecer la pared de la cápsula. Luego, se filtraron a través de un papel
Whatman n.o 1 y se lavaron con solución tampón (acetato acético, pH 5,5) para eliminar el exceso de iones en la superficie.
II.3. Diseño experimental
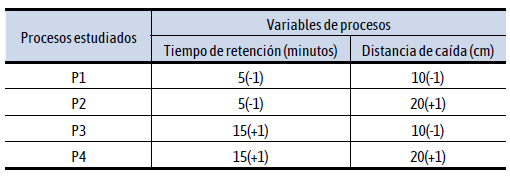
Para analizar el efecto de las variables de producción (tiempo de retención y distancia de caída) en la liberación del aceite esencial de orégano (ca) encapsulado, se estableció un diseño factorial 22. Se adoptaron dos niveles para la distancia de caída (10-20 cm) y dos para el tiempo de retención en la solución de cloruro de calcio (5-15 min). De las combinaciones de los niveles de variables independientes, se obtuvieron cuatro procesos de trabajo (Tabla 1).
Tabla 1. Procesos probados y niveles codificados para el tiempo de retención
y la distancia de caída

II.4. Secado de la cápsula
Las cápsulas se secaron en una estufa de convección forzada a dos temperaturas (35 °C y 65 °C), hasta peso constante. Las cápsulas secas se envasaron en recipientes sellados, se envolvieron en papel de aluminio y se almacenaron en un desecador por 48 hs, para luego ser analizadas.
II.5. Caracterización de cápsulas
Contenido de humedad: se midió el método gravimétrico, en estufa a 105 ºC hasta peso constante (aoac, 1998).
Actividad de agua (aw): utilizando el método higrométrico en el equipo HygroLab 2 (Rotronic, Alemania) a 25 °C.
Diámetro: se midió utilizando un micrómetro manual digital de 0-25 mm ± 0.001 mm (Time, Argentina).
Contenido total de polifenoles: se disolvió una cantidad conocida de cápsulas en citrato de sodio (5 % p/v) durante 3 hs en un agitador Orbit-Environ (Lab- Line Instruments, ee.uu.) a 37 °C y 125 rpm. El citrato de sodio actúa como un
quelante al disgregar por completo el gel de alginato de calcio (Draget, 2009). El contenido de polifenoles totales se cuantificó utilizando el método de Folin- Ciocalteau, midiendo la absorbancia en un espectrofotómetro UV/Visible (Libra S22) a 765 nm (Dambolena et al., 2009). La concentración expresada como meq de ácido gálico/ml de aeo.
II.6. Eficiencia de encapsulación
Para determinar el contenido de aceite superficial se procedió a pesar 0.5 g de cápsulas, colocándolas en un tubo de ensayo, con 4 ml de hexano, como solvente de extracción y 1 ml agua. Mediante agitación en un vortex por 15 min. Posteriormente fueron centrifugadas por 10 min en un tubo graduado cuantificando el sobrenadante. Para cuantificar el aceite interno se disolverán las cápsulas en una solución de citrato de sodio al 5 %, usando agitador magnético a 37 °C y durante 3 horas. La cantidad de aceite esencial se determinará midiendo la cantidad de polifenoles en la solución de citrato de sodio por la técnica de Folin- Ciocalteu.
II.7. Liberación de aceite esencial de orégano
La técnica seleccionada para determinar la liberación del ca fue mediante hinchamiento; se realizó con el propósito de evaluar el daño o degradación que puede ocurrir en la cápsula, quedando expuesta en algún sistema con alto contenido de humedad. Este mecanismo consiste en colocar las cápsulas en un medio termodinámicamente compatible, en este caso agua destilada, donde el polímero se hincha debido a la adsorción del medio y el ca puede difundirse a través de la zona de la matriz que ha experimentado hinchamiento (Deladino et al., 2008). El ensayo se llevó a cabo con un 1 gramo de cápsulas, obtenidas en los diferentes procesos, las cuales se sumergieron en diferentes tubos de ensayo que contenían 5 ml de agua destilada con agitación continúa a temperatura ambiente durante 48 hs. El ensayo se realizó por quintuplicado para cada uno de los procesos.
El porcentaje de liberación del aceite esencial de orégano se calculó a partir de la concentración de polifenoles cuantificada por la técnica de Folin-Ciocalteu, descrita previamente en las cápsulas, usando la ecuación:
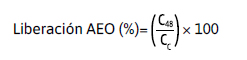
donde C48 corresponde a polifenoles totales liberados a las 48 hs y Cc corresponde a polifenoles totales encapsulados empleado en formulación de las cápsulas.
III. Análisis estadístico
El software InfoStat versión 2008 (Di Rienzo et al., 2011) se utilizó para todos los análisis estadísticos. El análisis de varianza (anova) y el análisis de regresión se aplicaron con un nivel de significancia de 0,05. Se utilizó la prueba de Fisher (lsd Fisher) para comparar medias.
IV. Resultados y discusión
IV.1. Encapsulación del aceite esencial de orégano
Cápsulas de secado
La temperatura de secado seleccionada fue a 65 °C, porque mantuvo la forma esférica de las cápsulas, teniendo en cuenta que las temperaturas más altas del aire aceleran la velocidad de secado de las mismas, promoviendo una formación rápida de la corteza; así se proporciona una membrana firme alrededor de las partículas, evitando una mayor lixiviación del aceite. Las curvas de secado mostraron tiempos entre 70 a 100 minutos (Figura 1). Las cápsulas obtenidas por los procesos P1, P2 y P4 tenían un contenido de humedad inicial mayor que las cápsulas obtenidas por el proceso P3, a su vez, en las cápsulas obtenidas por el proceso P1 el contenido de humedad siempre fue más alto a lo largo de la curva, mostrando el tiempo más largo para alcanzar equilibrio. Un material de pared debe tener perfiles de secado adecuados para lograr una rápida formación de una pared densa y una buena protección del núcleo (Gharsallaoui et al., 2007).
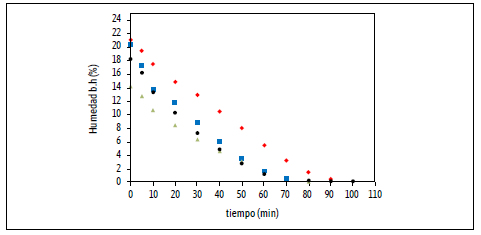
Figura 1. Secado de curvas a 65 °C de cápsulas de alginato con oea para los diferentes procesos (P1 ; P2 ; P3 ; P4)
IV.2. Caracterización
El contenido de humedad, la actividad del agua y el diámetro de las cápsulas con aceite esencial de orégano, obtenidas en los diferentes procesos estudiados se muestran en la Tabla 2.
Tabla 2. Valores de humedad, actividad de agua y diámetro de cápsulas con aceite esencial de orégano
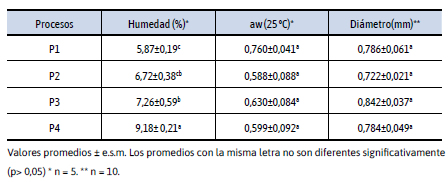
Los valores del contenido de humedad son superiores al 5 %, con diferencias significativas (p<0.05) entre los procesos, son valores similares a los reportados para cápsulas de alginato (Hernández Dávila, 2015). Al mismo tiempo, el contenido de humedad de las cápsulas se encuentra cerca de las especificaciones de humedad mínima para polvo seco en la industria alimentaria que está entre 3 y 4 g/100 g de agua (Klaypradit, y Huang, 2008, Huang et al., 2014). El valor más alto del contenido de humedad fue para los niveles más altos de ambas variables (tiempo-distancia), mientras que los contenidos de humedades de los procesos P2 y P3, y los procesos P1 y P2 no fueron significativamente diferentes (p> 0,05 ), siendo el valor más bajo para las cápsulas obtenidas por el proceso de menor tiempo de retención y menor distancia (P1). Los procesos no fueron significativamente influyentes (p>0,05) en el valor de la actividad del agua y el diámetro de las cápsulas (Tabla 2). Los valores de actividad de agua son más altos que los reportados para cápsulas de caseinato de sodio (aw: entre 0,091 y 0,153) (González Montes, 2012) y los reportados para cápsulas de alginato de sodio secas de extractos liofilizados de yerba mate inmersos por 15 minutos en quitosano (0,330 ± 0,009) (Deladino et al., 2008). Los valores de diámetro de las cápsulas con aceite esencial de orégano fueron mayores que los tamaños informados para las cápsulas de alginato con aceite esencial de orégano y para las cápsulas de aceite de salvia (García, 2015).
IV.3. Contenido total de polifenoles en cápsulas
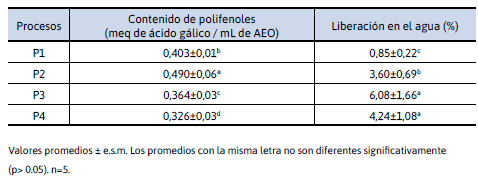
El contenido total de polifenoles en las cápsulas refleja la cantidad de aceite esencial de orégano dentro de las cápsulas y el grado en que la matriz puede evitar la difusión de material interno a través de la pared (Fuentes-Ortega et al., 2017). La Tabla 3 muestra las concentraciones de polifenoles presentes (meq de ácido gálico/mL de aeo) en las cápsulas, donde se observó que hay una diferencia significativa entre los diferentes procesos (p<0,05). Los resultados muestran que un aumento en el tiempo de retención a la misma distancia de caída, la concentración de polifenoles presente en las cápsulas disminuye significativamente. En cambio, si se mantiene constante el tiempo de retención y se aumenta la distancia de caída tienen comportamientos diferentes, en el tiempo de retención más corto, a mayor distancia de caída produce cápsulas con una mayor concentración de polifenoles, es decir, más aceite esencial de orégano. Esto podría deberse a que se forma un gel más fuerte que retiene más el ca. Por otro lado, a un mayor tiempo de retención, el aumento en la distancia de caída provoca una disminución en la concentración de polifenoles, siendo el proceso que forma las cápsulas con la menor cantidad de aceite esencial.
Tabla 3. Concentraciones de polifenoles en cápsulas y valores del porcentaje de liberación del aceite esencial de orégano de las cápsulas en agua
IV.4. Eficiencia de encapsulación
En la Figura 2 se observan los resultados para porcentaje de eficiencia de encapsulación en los distintos procesos estudiados. Donde se observan los valores más altos de %EE corresponden a los procesos de menor distancia de goteo, siendo el de mayor valor el de más tiempo de retención en la solución de cloruro de calcio. Por otro lado, los valores más bajos de eficiencia corresponden a los de mayor distancia de goteo, los cuales no presentaron diferencia significativa (p > 0,05). Los resultados muestran que cuando la distancia de goteo es mayor, el tiempo de retención no es un factor influyente en la eficiencia de escapulado, pero no es conveniente un aumento de distancia entre la salida de la gota y la solución de cloruro de calcio. Según los porcentajes calculados de la eficiencia del encapsulado, la mejor combinación de las variables sería el de los niveles más bajo de tiempo y distancia.
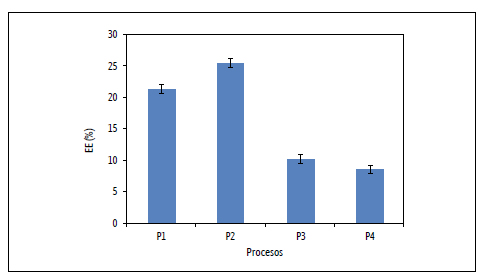
Figura 2. Porcentaje de Eficiencia de encapsulado
Columnas con una letra común no son significativamente diferentes (p > 0,05) n=3.
IV.5. Liberación en agua de aceite esencial de orégano
El hinchamiento de la cápsula es un factor importante para controlar la velocidad de liberación de un compuesto activo, ya que afecta la permeabilidad de la cápsula, el área superficial disponible para el contacto con la solución circundante y también la concentración intracapsular cuando el ca se diluye dentro de la cápsula. Por lo tanto, la velocidad de liberación del aceite esencial de orégano dependerá de la capacidad de hinchamiento de la cápsula de alginato.
Los valores de la liberación en agua del aceite esencial de orégano de las cápsulas a través de la medición de los polifenoles totales presentes en dicho compuesto se muestran en la Tabla 3. La liberación se calculó en base al aceite esencial de orégano atrapado. De acuerdo con el análisis estadístico, la variable de tiempo (p = 0,0022) mostró que existen diferencias significativas entre los valores del porcentaje de liberación, mientras que la variable de distancia de caída (p = 0,0017) no presentó diferencias significativas. Al observar la interacción de las variables, se muestra que en un tiempo de retención más corto, el aumento en la distancia de caída provoca una mayor liberación del compuesto activo. A su vez, aumentar el tiempo de retención (15 min) independientemente de la distancia de caída aumenta su liberación.
Teniendo en cuenta que el mecanismo de liberación de aceite esencial de orégano está controlado principalmente por el hinchamiento de la cápsula de alginato en la etapa inicial (Pasparakis y Bouropoulos, 2006), se puede deducir que las cápsulas que sufren más hinchazón son las que se obtienen del mayor tiempo de retención. El hinchamiento de las cápsulas secas se atribuye principalmente a la hidratación de los grupos hidrófilos de alginato (Hoffman, 2012). En este caso, el agua libre penetra dentro de las cápsulas con el fin de llenar los poros inertes entre las cadenas de polímero, lo que contribuye a un mayor grado de hinchazón. Conseguir el mejor proceso para obtener una encapsulación adecuada del aceite esencial de orégano es de primordial importancia para preservar su actividad antioxidante, aumentar la vida útil y estudiar su liberación en diferentes momentos. Por otro lado, cabe destacar que el porcentaje de liberación del compuesto activo no supero el 6 %, lo que podría decirse que las capsulas en un sistema con alta humedad tendrían una alta retención o, en caso contrario, si se persigue producir una liberación más rápida se debería ensayar otro mecanismo.
V. Conclusión
En conclusión, el contenido calculado de polifenoles del aceite esencial de orégano de la especie Origanum majorana fue superior a los comparados con los datos bibliográficos, así como su poder antioxidante, en las condiciones estudiadas. En referencia a la evaluación de alginato de sodio como material encapsulante, las cápsulas con mayor contenido de polifenoles, es decir, aquellas que retuvieron la mayor cantidad de aceite esencial, fueron las obtenidas por proceso
de mayor distancia entre la salida de la gota y la solución de cloruro cálcico, y el tiempo de retención más corto; mientras que las cápsulas sufrieron más hinchazón, fueron las obtenidas por procesos de mayor tiempo de retención.
Por otro lado, es interesante mencionar que los aceites esenciales podrían ser útiles como fuentes dietéticas de antioxidantes naturales para mejorar la nutrición y la salud humana, donde la tecnología de encapsulación, podría proporcionar ventajas para la preservación de sustancias susceptibles a la oxidación y contribuir a la incorporación de compuestos con actividad antioxidante en los alimentos.
Referencias bibliográficas
1. AOAC (1998). Official Methods of Analysis, 16th ed., 4th Revision. Association of Official Analytical Chemists, New York.
2. Bozin, B.; Mimica-Dukic, N.; Simin, N.; Anackov, G. (2006). Characterization of the volatile composition of essential oils of some Lamiaceae spices and the antimicrobial and antioxidant activities of the entire oils. Journal of agricultural and food chemistry, 54(5), 1822-1828.
3. Celiktas, O. Y.; Kocabas, E. H.; Bedir, E.; Sukan, F. V.; Ozek, T.; Baser, K. H. C. (2007). Antimicrobial activities of methanol extracts and essential oils of Rosmarinus officinalis, depending on location and seasonal variations. Food Chemistry, 100(2), 553-559.
4. Champagne, C. P.; Fustier, P. (2007). Microencapsulation for the improved delivery of bioactive compounds into foods. Current opinion in biotechnology, 18(2), 184-190.
5. Dadalioğlu, I.; Evrendilek, G. A. (2004). Chemical compositions and antibacterial effects of essential oils of Turkish oregano (Origanum minutiflorum), bay laurel (Laurus nobilis), Spanish lavender (Lavandula stoechas L.), and fennel (Foeniculum vulgare) on common foodborne pathogens. Journal of agricultural and food chemistry, 52(26), 8255-8260.
6. Dambolena, J. S.; Zunino, M. P.; Lucini, E. I.; Olmedo, R.; Banchio, E.; Bima, P. J.; Zygadlo, J. A. (2009). Total phenolic content, radical scavenging properties and essential oil composition of Origanum species from different populations. Journal of Agricultural and Food Chemistry, 58(2), 1115-1120
7. Deladino, L.; Anbinder, P. S.; Navarro, A. S.; Martino, M. N. (2008). Encapsulation of natural antioxidants extracted from Ilex paraguariensis. Carbohydrate Polymers, 71(1), 126-134.
8. Di Rienzo, J.A.; Casanoves, F.; Balzarini, M.G.; Gonzalez, L.; Tablada, M.; Robledo, C.W. (2011). InfoStat. Universidad Nacional de Córdoba.
9. Draget, K. I. (2009). Alginates. In Handbook of hydrocolloids. Woodhead Publishing, pp. 807-828.
10. Fuentes-Ortega, T.; Martínez-Vargas, S. L.; Cortés-Camargo, S.; Guadarrama-Lezama, A. Y.; Gallardo-Rivera, R.; Baeza-Jimenéz, R.; Pérez-Alonso, C. (2017). Effects of the process variables of microencapsulation sesame oil (sesamum indica l.) by spray drying. Revista Mexicana de Ingeniería Química, 16(2).
11. Funami, T.; Fang, Y.; Noda, S.; Ishihara, S.; Nakauma, M.; Draget, K. I.; Nishinar, K.; Phillips, G. O. (2009). Rheological properties of sodium alginate in an aqueous system during gelation in relation to supermolecular structures and Ca2+ binding. Food Hydrocolloids, 23(7), 1746-1755.
12. García, M. F. (2015). Encapsulación de aceites esenciales funcionales para su aplicación en agricultura. Disertación Doctoral, Universidad Politécnica de Valencia.
13. Gharsallaoui, A.; Roudaut, G.; Chambin, O.; Voilley, A.; Saurel, R. (2007). Applications of spray-drying in microencapsulation of food ingredients: An overview. Food Research International, 40(9), 1107-1121.
14. González-Molina, E., Domínguez-Perles, R., Moreno, D. A., García-Viguera, C. (2010). Natural bioactive compounds of Citrus limon for food and health. Journal of pharmaceutical and biomedical analysis, 51(2), 327-345.
15. González Montes, C. (2012). Evaluación fisicoquímica y capacidad antioxidante del aceite de amaranto (Amaranthus hypochondriacus) y estabilidad oxidativa de diferentes sistemas de encapsulación. Disertación Doctoral.
16. Guimarães, R.; Sousa, M. J.; Ferreira, I. C. (2010). Contribution of essential oils and phenolics to the antioxidant properties of aromatic plants. Industrial Crops and Products, 32(2), 152-156.
17. Hernández Dávila, C. A. (2015). Elaboración y caracterización de Microcápsulas mediante Gelificación Iónica externa, de la fracción alcaloidea de ilex guayusa con alginato sódico, y su utilización en la formulación de una forma de dosificación sólida. .Bachelor’s thesis, Escuela Superior Politécnica de Chimborazo.
18. Hoffman, A. S. (2012). Hydrogels for biomedical applications. Advanced drug delivery reviews, 64, 18-23.
19. Huang, H.; Hao, S.; Li, L.; Yang, X.; Cen, J.; Lin, W.; Wei, Y. (2014). Influence of emulsion composition and spray-drying conditions on microencapsulation of tilapia oil. Journal of food science and technology, 51(9), 2148-2154.
20. Klaypradit, W.; Huang, Y. W. (2008). Fish oil encapsulation with chitosan using ultrasonic atomizer. LWT-Food Science and Technology, 41(6), 1133-1139.
21. Lagouri, V.; Blekas, G.; Tsimidou, M.; Kokkini, S.; Boskou, D. (1993). Composition and antioxidant activity of essential oils from oregano plants grown wild in Greece. Zeitschrift für Lebensmitteluntersuchung und-Forschung A, 197(1), 20-23.
22. Pasparakis, G.; Bouropoulos, N. (2006). Swelling studies and in vitro release of verapamil from calcium alginate and calcium alginate–chitosan beads. International journal of pharmaceutics, 323(1), 34-42.
23. Pizzale, L.; Bortolomeazzi, R.; Vichi, S.; Überegger, E.; Conte, L. S. (2002). Antioxidant activity of sage (Salvia officinalis and S fruticosa) and oregano (Origanum onites and O indercedens) extracts related to their phenolic compound content. Journal of the Science of Food and Agriculture, 82(14), 1645-1651.
24. Shahidi, F., Han, X. Q. (1993). Encapsulation of food ingredients. Critical Reviews in Food Science & Nutrition, 33(6), 501-547.